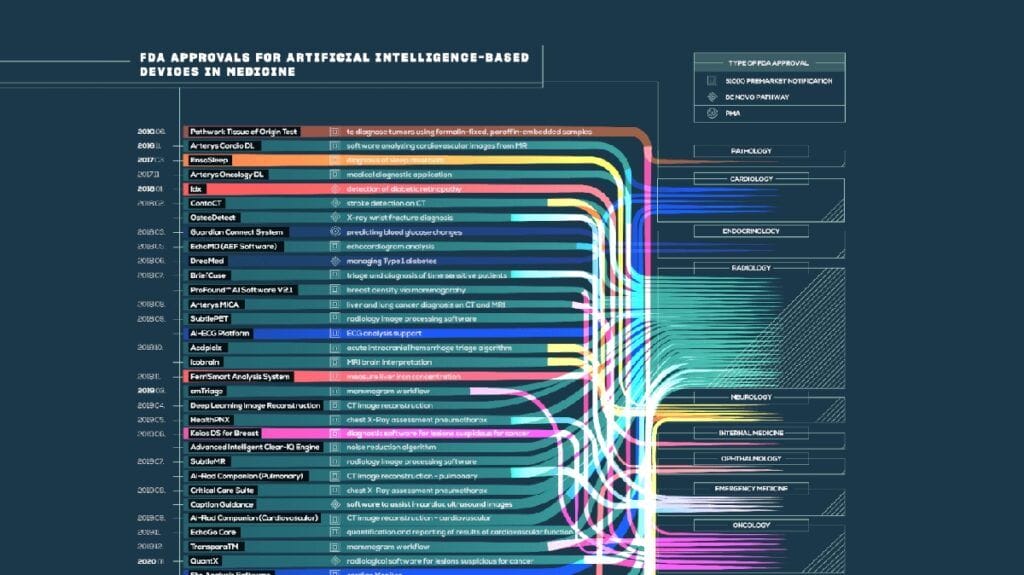
El estado de la Inteligencia Artificial en la sanidad
La Inteligencia Artificial ha provocado un giro radical en diversas áreas, incluyendo el sector de la salud. Actualmente, tenemos casi 700 dispositivos médicos basados en IA aprobados por la FDA que certifican esta creciente revolución. Entre estos dispositivos encontramos el Software como Dispositivo Médico (SaMD), componente esencial en el panorama de la salud digital.
Las tecnologías de IA se han adaptado a un amplio espectro de campos clínicos, la mayoría de los cuales brindan asistencia. En entornos de atención aguda en países de alto ingreso, es habitual que los médicos empleen sistemas de IA para validar o respaldar la información o las decisiones proporcionadas por la IA. Estos sistemas se integran con los sistemas de información clínica existentes, como los registros médicos electrónicos, y tienen la capacidad de procesar enormes cantidades de datos genómicos, de biomarcadores y fenotípicos.[automatic_youtube_gallery type="search" search="El Estado de la IA en la Atención Médica" cache="2419200" per_page="1" thumb_excerpt="0" player_description="0"]
La IA se ha integrado sin problemas en los sistemas clínicos para la detección de hallazgos, propuestas de diagnósticos y recomendaciones de tratamientos en especialidades intensivas en datos como radiología, patología y oftalmología. Sin embargo, la implementación de IA en entornos clínicos entraña desafíos propios, como la necesidad de que los sistemas de IA se generalicen a situaciones no contempladas a priori en los datos de entrenamiento.
El papel de la FDA en la regulación de los dispositivos médicos basados en IA
La Administración de Alimentos y Medicamentos de EE.UU. (FDA) juega un papel crítico en la regulación de los dispositivos médicos basados en IA. El proceso de aprobación de la FDA para estos dispositivos a menudo implica el uso de planes de control de cambios predefinidos (PCCP) en las presentaciones comerciales para optimizar el proceso. La FDA no regula el uso o el mantenimiento de dispositivos antiguos, lo que conlleva ciertos riesgos de ciberseguridad.
La FDA se compromete a apoyar el uso de Tecnologías de Salud Digital (DHT) en el desarrollo de medicamentos clínicos y ha desarrollado un programa integral para interactuar con las partes interesadas en esta importante área científica. Esto incluye un marco para el uso de DHT en el desarrollo de productos farmacéuticos y biológicos, talleres, proyectos de demostración, reuniones públicas/talleres y orientaciones relacionadas.
El año pasado, la FDA publicó una guía preliminar sobre la ciberseguridad de los dispositivos médicos, debido a las crecientes vulnerabilidades en el software y el firmware que alimentan los dispositivos médicos. Actualmente, la FDA está elaborando una guía para dispositivos habilitados para IA y aprendizaje automático que requieren planes de control de modificaciones en las presentaciones comerciales.
Desafíos y expectativas futuras
Con más del 35% de las empresas utilizando AI a diario, aumenta la demanda de regulación de la IA en la salud. Los desafíos y riesgos de regular la IA en la salud incluyen la gestión de datos médicos sensibles, el sesgo en las decisiones de IA, la transparencia en los algoritmos de IA e integrarlos en los sistemas de salud existentes.
Mientras que USA todavía está buscando un enfoque regulatorio para la IA en la salud, y algunos estados han aprobado leyes limitando su uso, la UE lidera en la mayoría de los aspectos de la regulación de la IA en la sanidad. La UE está trabajando activamente en la primera Ley de IA integral, con un enfoque en privacidad, transparencia y responsabilidad.
A medida que avanzamos, será interesante observar cómo evoluciona el panorama regulatorio para acomodar las tecnologías de IA en rápido avance, garantizando su uso seguro y efectivo en la industria de la salud.
